Sabak Wioletta
Zakład Dydaktyczny Chemii Organicznej i Technologii Chemicznej
Pracownia Peptydów
Foldamery oligomocznikowe i mocznikowo-g-amidowe
Wioletta Sabak
Promotor: dr Karolina Pułka-Ziach
Foldamery to nienaturalne oligomery, które przyjmują dobrze zdefiniowane, specyficzne i przewidywalne struktury drugorzędowe, np. helisy i b-kartki. [1] Różnorodność budowy szkieletów foldamerów jest wyjątkowo duża, począwszy od aromatycznych oligoamidów kończąc na nienaturalnych aminokwasach (b- lub g-aminokwasy). [2] Oligomoczniki i ich pochodne również należą do rodziny foldamerów. Tworzą stabilne helisy typu 2.5 w rozpuszczalnikach organicznych, w środowisku wodnym, a także w ciele stałym. [3]
Celem mojej pracy magisterskiej było opracowanie syntezy oligomoczników z grupą tiolową na C-końcu oraz hybryd mocznikowo-g-amidowych z grupa tiolową na N-końcu (Rys.1). Pierwszy etap pracy polegał na otrzymaniu karbaminianowych bloków budulcowych z grupą N3 jako zamaskowanej grupy aminowej oraz Fmoc-g-aminokwasów. Związkami wyjściowymi w obu syntezach były Boc-a-aminokwasy.
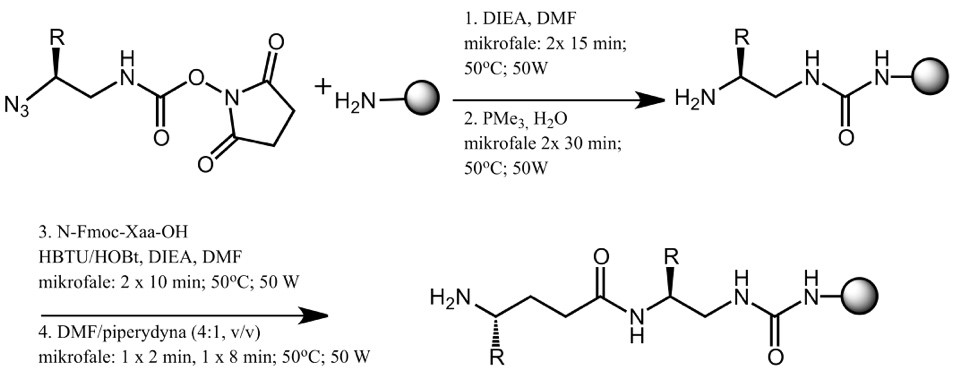
Rys.1 Ogólny schemat syntezy foldamerów oligomocznikowych i ich pochodnych na nośniku stałym.
Synteza foldamerów o pożądanej długości prowadzona była na nośniku stałym w środowisku mikrofal, a poszczególne etapy sprawdzane były za pomocą testu chloranilowego. Oligomoczniki z grupą SH na C-końcu próbowano otrzymać na żywicy cysteamino-2-chlorotrytylowej (o różnym podstawieniu) oraz TentaGel S chlorotrytylowej. Niestety, dotychczas nie udało się otrzymać zamierzonych związków.
Synteza hybryd mocznikowo-g-amidowych z grupą –SH na N-końcu prowadzona była na żywicy amidowej Rinka typu NovaPeg. Otrzymano z powodzeniem zaplanowane związki. Uzyskane foldamery posłużą jako związki modelowe do badania transportu elektronów, co może przyczynić się do zgłębienia wiedzy na temat skomplikowanych mechanizmów reakcji biologicznych.
Literatura:
[1] Gellman S., Foldamers: A manifesto, Acc. Chem. Res. 1998, 31, 173-180.
[2] Guichard G., Huc I., Synthetic foldamers, Chem.Commun., 2011, 47, 5933-5941.
[3] Nelli Y., Fisher L., Collie G., Kauffmann G., Guichard G., Structural Characterization of Short Hybrid Urea/Carbamate (U/C) Foldamers: A case of Partial Helix Unwinding, Peptide Science, 2013, 6, 693-697.