Pacner Sandra
Zakład Chemii Organicznej i Technologii Chemicznej
Pracownia Syntezy Nanomateriałów Organicznych i Biomolekuł
Synteza niesymetrycznych disulfidów 6-tioguanozyny
Sandra Pacner
Promotor: dr. hab. Marzena Jankowska-Anyszka
6-tioguanozyna to nukleozyd, zawierający modyfikację w obrębie guaniny, polegającą na zastąpieniu atomu tlenu w pozycji 6-tej atomem siarki. Znajdująca się w nukleozydzie 6-tioguanina znalazła zastosowanie w medycynie między innymi jako lek przeciwnowotworowy. Jej działanie cytostatyczne zostało potwierdzone w przypadku kilku postaci białaczki: ostrej białaczki szpikowej i ostrej białaczki limfoblastycznej [1]. Obecność grupy tiolowej w cząsteczce 6-tioguanozyny jest interesująca z chemicznego punktu widzenia, ponieważ pozwala na utworzenie mostka disiarczkowego. Wiele związków, posiadających to ugrupowanie, znalazła zastosowanie w medycynie na przykład jako środki antynowotworowe, antykrzepliwe, przeciwcukrzycowe oraz leki stosowane w zwalczaniu infekcji bakteryjnych i grzybiczych [2],[3],[4]. Zdolność związków, zawierających grupę sulfhydrylową np. glutationu, do tworzenia mostka disiarczkowego w warunkach utleniających i jego rozpadu w warunkach redukujących jest wykorzystywana w organizmach do utrzymania odpowiednich warunków utleniająco-redukcyjnych w komórce.
Celem pracy magisterskiej jest synteza niesymetrycznych disulfidów alifatycznych i aromatycznych 6-tioguanozyny z zastosowaniem metody wykorzystującej czynnik utleniający TCCA (kwas trichlorocyjanurowy) [5]. Do cząsteczki 6-tioguanozyny poprzez mostek disulfidowy mogą zostać wprowadzone związki pełniące funkcję sondy molekularnej, np. znaczniki fluorescencyjne. Taka modyfikacja nukleozydu umożliwiłaby lokalizację i oznaczenie stężenia związku w komórkach zwierzęcych. Niesymetryczne disulfidy 6-tioguanozyny, w połączeniu z możliwością redukcji wiązań disulfidowych w naturalnych warunkach komórki, otwierają drogę na wprowadzenie potencjalnych leków do organizmu.
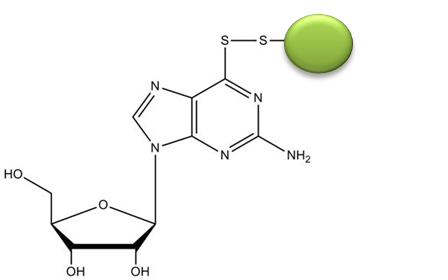
Rys.1. Struktura niesymetrycznego disulfidu 6-tioguanozyny.
Literatura:
[1] A. Kowalska, Chlorowcowe i siarkowe pochodne naturalnych zasad purynowych o aktywności przeciwnowotworowej i immunosupresyjnej, Farmaceutyczny Przegląd Naukowy, 2009, 5, 15-20.
[2] G. Whiesides, Thiol-disulfide interchange, Department of Chemistry, Harvard university, Cambrtdge, 1993, 13, 634-658.
[3] E. Block, R. DeOrazio, and M. Thiruvazhi, Simple Total Syntheses of Biologically Active Pentathiadecane Natural Products, 2,4,5,7,9-Pentathiadecane 2,2,9,9-Tetraoxide (Dysoxysulfone), from Dysoxylum richii, and 2,3,5,7,9-Pentathiadecane 9,9-Dioxide, the Misidentified Lenthionine Precursor SE-3 from ShiitakMushroom (Lentinus edodes), J. Org. Chem., 1994, 59, 9, 2273-2275.
[4] S. Kohlmünzer, Farmakognozja: podręcznik dla studentów farmacji. Wyd. V unowocześnione. Warszawa: Wydawnictwo Lekarskie PZWL, 2003, 669.
[5] F. Yang, W. Wang, K. Li, W. Zhao, X. Dong, Efficient one-pot construction of unsymmetrical disulfide bonds with TCCA, Tetrahedron Letters, 2016.