Nalewajko Olga
Zakład Chemii Fizycznej i Radiochemii
Pracownia Elektrochemicznych Źródeł Energii, Grupa badawcza Radiochemii dla Medycyny i Przemysłu
Enzymatyczna synteza bromopochodnych L-fenyloalaniny selektywnie znakowanych izotopami wodoru
Olga Nalewajko
Promotor: dr Katarzyna Pałka
Fenyloketonuria (PKU), jest chorobą genetyczną wywołaną zaburzeniami metabolizmu aminokwasów. Za jej przyczynę uważa się brak lub niedobór enzymu hydroksylazy fenyloalaninowej, PAH, (Phenylalanine hydoxylase). W zdrowym organizmie prawie 75% L-Phe ulega przekształceniu w L-Tyr, a około 25% służy do budowy białek. U osób chorych przekształcenie L-Phew L-Tyr jest zahamowane, czego skutkiem jest gromadzenie jej we wszystkich płynach ustrojowych.
Wciąż niewielka jest wiedza na temat wielu chorób metabolicznych, nowotworowych i neurodegeneracyjnych, dlatego korzystne staje się poznanie mechanizmów reakcji enzymatycznych, w których bierze udział między innymi L-fenyloalanina.
Jedną z lepiej znanych biokonwersji jest wykorzystanie kwasu trans-cynamonowego i enzymu amoniakoliazy L-fenyloalaninowej (PAL). Enzym otrzymuje się z wielu źródeł roślinnych i drobnoustrojów, w tym z drożdży, Rhodotorula glutinis. Enzym PAL nie wymaga stosowania żadnych kofaktorówi katalizuje nieoksydatywną deaminację L-fenyloalaniny do kwasu trans-cynamonowego i jonów amonowych, jak również reakcję odwrotną, która jest szczególnie interesująca dla chemików.
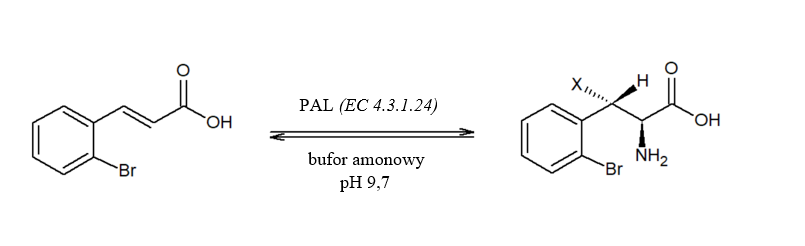
Enzymatyczną syntezę aminokwasów, znakowanych stabilnymi izotopami, w tym deuterem (2H) lub trytem (3H) stosuje się do poznania mechanizmu niektórych reakcji, a także jest odpowiednia do zastosowań biomedycznych i diagnostyki klinicznej. Przeprowadzone przeze mnie syntezy związków znakowanych mogą zostać wykorzystane w późniejszym czasie na potrzeby medycyny nuklearnej, zwłaszcza w pozytonowej tomografii emisyjnej (PET), w której wykorzystuje się związki znakowane krótkotrwałymi emiterami promieniowania β+ ( zwłaszcza brom- 76).