Stemler Monika
Zakład Chemii Organicznej i Technologii Chemicznej
Pracownia Syntezy Nanomateriałów Organicznych i Biomolekuł
Synteza pronukleotydów opartych o monofosforanowe analogi kapu
Monika Stemler
Promotor: dr hab. Marzena Jankowska – Anyszka
Opiekun: dr Karolina Piecyk
Na końcu 5’ mRNA znajduje się charakterystyczna struktura zwana kapem. Zbudowana jest ona z 7 – metyloguanozyny połączonej mostkiem trifosforanowym z łańcuchem mRNA. Kap pełni w komórce wiele ważnych funkcji. Ze względu na prowadzone przeze mnie badania najbardziej interesującą z nich jest inicjacja procesu translacji. Rozpoczęcie syntezy łańcucha polipeptydowego białek na matrycy mRNA związane jest z koniecznością rozpoznania struktury kapu przez białko eIF4E. Etap ten limituje proces translacji. W komórkach, w których znajdują się cząsteczki mRNA kodujące białka onkogenne, stężenie czynnika inicjującego translację (eIF4E) jest podwyższone. Analogi kapu o zwiększonym powinowactwie do eIF4E mogą wiązać jego nadmiar, dzięki czemu zahamują one translację białek nowotworowych. Do tej pory zsyntetyzowano wiele analogów końca 5’ mRNA o potencjalnym znaczeniu terapeutycznym. Problemem jest jednak ich transport przez błonę komórkową, co związane jest z obecnością ładunków ujemnych w obrębie grup fosforanowych tych cząsteczek. Celem mojej pracy jest synteza monofosforanowych inhibitorów kapu z modyfikacją na grupie fosforanowej [Rysunek 1].
Syntezowane związki:
a) podstawione są w pozycji N2 [1], co zwiększa ich powinowactwo do czynnika 4E w stosunku do bazowej struktury kapu
b) przekształcone są w amidofosfodiestry [2, 3], co prowadzi do zamaskowania ładunków ujemnych
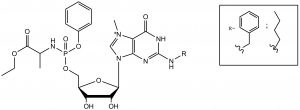
Rysunek 1. Struktura syntetyzowanych związków
Otrzymane w ramach pracy magisterskiej związki zostaną w kolejnym etapie badań poddane analizie przepuszczalności przez błonę komórkową, a najbardziej obiecujące analogi badaniom in vivo.
Literatura:
[1] Piecyk K., Davis R.E., Janskowska – Anyszka M., Bioorganic & Medicinal Chemistry. 2012, 20, 4781–4789.
[2] Cho, J.H., Amblard F., Coats S.J., Schinazi R.F., Tetrahedron. 2011, 67, 5487–5493.
[3] McGuigan C., et al. Bioorganic & Medicinal Chemistry. 2005, 13, 3219–3227.