Chojnacki Rafał
Zakład Chemii Organicznej i Technologii Chemicznej
Pracownia Peptydów
Synteza i badania stabilności konformacyjnej foldamerów tiomocznikowo-mocznikowych
Rafał Chojnacki
Promotor: dr hab. Karolina Pułka-Ziach
Opiekun: mgr Paulina Bachurska
Jednym z ważnych i użytecznych elementów do badania związku między strukturą, a funkcją biologicznie czynnych oligomerów są izosteryczne modyfikacje łańcucha. W Pracowni Peptydów od kilku lat zajmujemy się foldamerami oligomocznikowymi. Foldamery to nienaturalne oligomery, które mają tendencję do przyjmowania stabilnych, dobrze zdefiniowanych i przewidywalnych struktur drugorzędowych. [1] Oligomoczniki zwijają się w stabilne helisy typu 2.5. [2] Jedną z ciekawych modyfikacji sekwencji foldameru oligomocznikowego pozwalającą na badanie wpływu podstawień izosteryczych na konformację jest zastąpienie wiązania mocznikowego wiązaniem tiomocznikowym. [3] Powoduje to wydłużenie wiązania podwójnego C=S w porównaniu do wiązania C=O. Dodatkowo atom siarki w grupie tiomocznikowej charakteryzuje się mniejszymi zdolnościami akceptorowymi dla wiązań wodorowych w porównaniu do atomu tlenu w grupie mocznikowej. Ponadto protony NH grupy tiomocznikowej charakteryzują się wyższą kwasowością niż protony grupy mocznikowej.
Celem projektu było opracowanie metod syntezy czterech oligomerów mocznikowo-tiomocznikowch, w których grupa tiomocznikowa znajduje się w środku lub na tzw. C-końcu sekwencji (Rysunek 1a) oraz zbadanie wpływu dodatków na stabilność konformacyjną otrzymanych związków. Zaprojektowane struktury posiadają dodatkowo grupę elektronoakceptorową (p-NO2Ph) na C-końcu powodującą zwiększenie kwasowości protonów wiązania mocznikowego lub tiomocznikowego. Badania stabilności konformacyjnej oligomerów przeprowadzono wobec dodatku DMSO oraz TBAOH i TBAF. Do badań zastosowano metodę 1H NMR, dichroizm kołowy (CD) oraz spektroskopię UV-Vis.
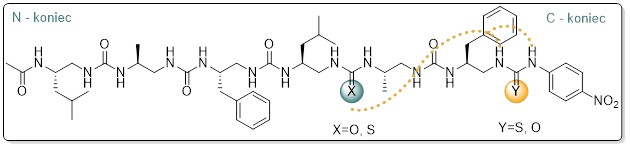
Rysunek 1. Struktura ogólna otrzymanych foldamerów tiomocznikowo-mocznikowych (żółtą przerywaną linią zaznaczono w jaki sposób tworzą się wewnątrzcząsteczkowe wiązania wodorowe)
Literatura:
[1] Gellman S., Acc. Chem. Res. 1998, 31, 173-180.
[2] Fischer L., Claudon P., Pendem N., Miclet E., Didierjean C., Ennifar E., Guichard G., Angew. Chem. Int. Ed. 2010, 49, 1067 –1070.
[3] Nelli Y., Antunes S., Salaün A., Thinon E., Massip S., Kauffmann B., Douat C., Guichard G., Chem. Eur. J. 2015, 21, 2870-2880.