Wójcik Radosław
Centrum Nowych Technologii Uniwersytetu Warszawskiego
Laboratorium Chemii Bioorganicznej
Synteza i badanie właściwości mononukleotydowych analogów końca 5’ mRNA zawierających podstawniki benzylowe przyłączone poprzez ugrupowanie 1,2,3-triazolowe do zasady azotowej
Radosław Wójcik
Promotor: prof. dr hab. Jacek Jemielity
Koniec 5’ mRNA (kap) jest ważną biologicznie strukturą zaangażowaną w proces ekspresji genów, co czyni go istotnym miejscem modyfikacji związanych z kontrolowaniem procesów metabolizmu RNA oraz produkcji białek. Dotychczasowe badania analogów tej struktury wykazały, że wprowadzenie ugrupowania triazolowego w obrębie łańcucha fosforanowego bądź zamiana grupy N7-metylowej na grupę benzylową może znacząco wpływać na ich właściwości biologiczne. Opisane w literaturze analogi wykazują zwiększone powinowactwo do białka inicjującego translację – eIF4E[1][2], zostały również scharakteryzowane jako małocząsteczkowe inhibitory 5’-nukleotydazy – cNIIIB[3].
Celem tego projektu magisterskiego było otrzymanie i charakteryzacja nowych analogów strukturalnych monofosforanu N7-metyloguanozyny, przy wykorzystaniu reakcji cykloaddycji azydkowo-alkinowej katalizowanej jonami miedzi(I) (CuAAC) należącej do grupy reakcji „click”. W ramach projektu zsyntezowano 19 nieopisanych wcześniej związków, w których do azotu N7 guanozyny poprzez linker metylenowy i ugrupowanie 1,2,3-triazolowe przyłączona była grupa benzylowa zawierająca dodatkowe podstawniki takie jak: atomy halogenów, grupy metylowe czy proste grupy funkcyjne.
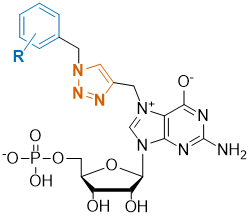
Rys. 1. Ogólna struktura otrzymanych związków
Wszystkie związki zostały scharakteryzowane technikami spektrometrii mas wysokiej rozdzielczości (HRMS) i magnetycznego rezonansu jądrowego (NMR). Przeprowadzono również szereg doświadczeń w celu sprawdzenia powinowactwa zsyntezowanych związków do enzymów z grupy fosfataz (hDcpS, hFhit, AtFhit), eksperymenty te umożliwiły weryfikację aktywności biologicznej otrzymanych analogów oraz pozwoliły na ocenienie czy zsyntezowane związki mogą być potencjalnymi inhibitorami dla enzymów związanych z metabolizmem nukleotydów.
Literatura:
[1] Walczak S., Sikorski P.J., Kasprzyk R., Kowalska J., Jemielity J., Org. Biolmol. Chem., 2018, 16, 6741.
[2] Brown C.J., McNae I., Fischer P.M., Walkinshaw M.D., J Mol Biol. 2007, 372(1), 7-15.
[3] Kozarski M., Kubacka D., Wojtczak B.A., Kasprzyk R., Baranowski M.R., Kowalska J., Bioorg. Med. Chem., 2017, 26(1), 191-199.