Piątkowski Jakub
Zakład Chemii Organicznej i Technologii Chemicznej
Pracownia Syntezy Metaloorganicznej
Synteza oraz charakterystyka zaktywowanych kompleksów rutenowych zawierających elektronoakceptorowe ugrupowanie sulfonamidowe
Jakub Piątkowski
Promotor: prof. dr hab. inż. Karol Grela
Opiekunowie: dr Louis Monsigny, dr inż. Anna Kajetanowicz
Reakcja metatezy olefin katalizowana alkilidenowymi kompleksami rutenu jest obecnie jednym z najpotężniejszych narzędzi w tworzeniu wiązań C(sp2)-C(sp2) we współczesnej syntezie organicznej.[1] Od momentu wprowadzenia stabilnego na szereg grup funkcyjnych tzw. katalizatora Grubbs’a pierwszej generacji (G-I),[2] reakcja ta znalazła szerokie zastosowanie w syntezie totalnej zaawansowanych strukturalnie związków organicznych, wliczając w to substancje czynne farmakologicznie, produkty naturalne, czy też dobrze zdefiniowane polimery.[3]
W celu uzyskania większej tolerancji na warunki atmosferyczne oraz zwiększonej aktywności w przemianach metatetycznych, dokonany został szereg modyfikacji strukturalnych – zamiana fosfiny na N-heterocykliczny karben[4] oraz modyfikacje części benzylidenowej.[5] Jedna z przełomowych modyfikacji polegająca na wprowadzeniu grupy nitrowej (N-II) do chelatującego liganda w tzw. katalizatorze Hoveydy-Grubbs’a (H-II) doprowadziła do dramatycznego wzrostu aktywności kompleksu w reakcji metatezy olefin.[6] Na przestrzeni lat, otrzymano szereg kompleksów z innymi grupami elektronoakceptorowymi,[7] których obecność prowadzi do osłabienia wiązania tlen-ruten, a co za tym idzie – szybszej aktywacji kompleksu. Niestety, synteza tychże kompleksów jest bardziej złożona, niż w przypadku macierzystego katalizatora Hoveydy-Grubbs’a.[8] Jednym z rozwiązań tego problemu jest znalezienie odpowiedniego bloku budulcowego, który przypomina strukturalnie benzylidenowy fragmentu kompleksu rutenowego, a co więcej – jest produktem pośrednim/ubocznym w dużoskalowym syntetycznym procesie technologicznym.
Celem projektu była synteza oraz charakteryzacja dwóch alkylidenowych kompleksów rutenowych (V-I, V-II) zawierających elektronoakceptorowe ugrupowanie sulfoamidowe we fragmencie benzylidenowym. Odpowiedni ligand użyty w wyżej wspomnianej syntezie otrzymany został na drodze jednej transformacji organicznej z dostępnego aldehydu będącego prekursorem komercyjnie dostępnego leku – Sildenafilu.[9]
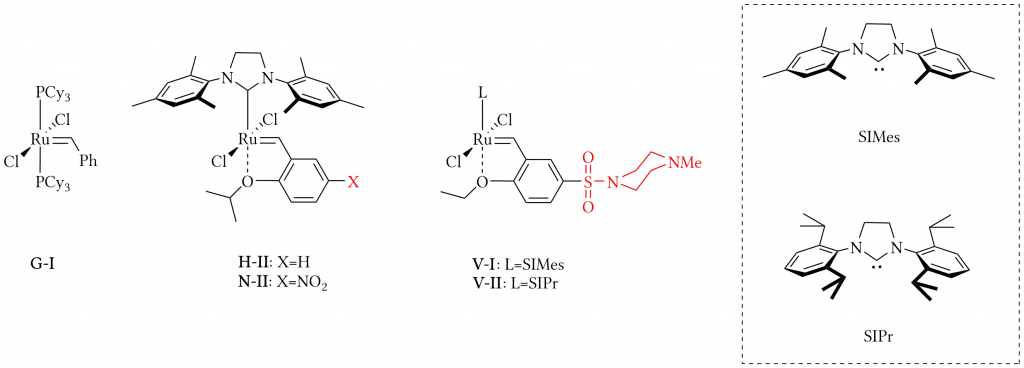
Schemat 1. Struktury komeryjnie dostępnych kompleksów (G-I, H-II, N-II) oraz będących obiektem badań niniejszej pracy (V-I, V-II).
Otrzymane kompleksy zostały zbadane oraz porównane z innymi komercyjnie dostępnymi katalizatorami pod kątem stabilności oraz aktywności w przemianach metatetycznych. Dokonano pełnej charakterystyki otrzymanych kompleksów przy pomocy szeregu metod spektroskopowych (1H oraz 13C NMR, IR), analitycznych (EA, HR-MS) oraz rentgenostrukturalnych (XRD). Dodatkowo, wykonano szereg eksperymentów mechanistycznych z wykorzystaniem spektroskopii UV-Vis, które ujawniły odmienny mechanizm aktywacji dla jednego z otrzymanych kompleksów.

Literatura:
[1] Vougioukalakis G. C., Grubbs R. H., Chem. Rev. 2010, 110, 1746.
[2] Schwab P., France M. B., Ziller J. W., Grubbs R. H., Angew. Chem. Int. Ed. 1995, 34, 2039.
[3] Grela K., Olefin Metathesis: Theory and Practice, Viley, Hoboken 2014.
[4] Scholl M., Ding S., Lee C. W., Grubbs R. H., Org. Lett. 1999, 1, 953.
[5] Kajetanowicz A., Grela K., Angew. Chem. Int. Ed. 2020, 59, 2.
[6] Grela K., Harutyunyan S., Michrowska A., Angew. Chem. Int. Ed. 2002, 41, 4038.
[7] Bieniek M., Bujok R., Milewski M., Arlt D., Kajetanowicz A., Grela K., J. Organomet. Chem. 2020, 918, 121276.
[8] Bujok R., Bieniek M., Masnyk M., Michrowska A., Sarosiek A., Stępowska H, Arlt D., Grela K., J. Org. Chem. 2004, 69, 6894.
[9] Bell A. S., Brown D., Terrett N. K., patent US 5250534A 1993.